Iklan
Pertanyaan
Benarkah reaksi-reaksi elektrode dalam sel elektrolisis mengikuti prioritas berikut? Gunakan data potensial elektrode standar dan gambar di bawah untuk mendukung pendapat Anda. Prioritas reaksi reduksi di katode: I. kation, II. air. Jika kation lebih mudah tereduksi daripada air, maka kation yang tereduksi. Jika sebaliknya, maka molekul air yang tereduksi.
Benarkah reaksi-reaksi elektrode dalam sel elektrolisis mengikuti prioritas berikut? Gunakan data potensial elektrode standar dan gambar di bawah untuk mendukung pendapat Anda.
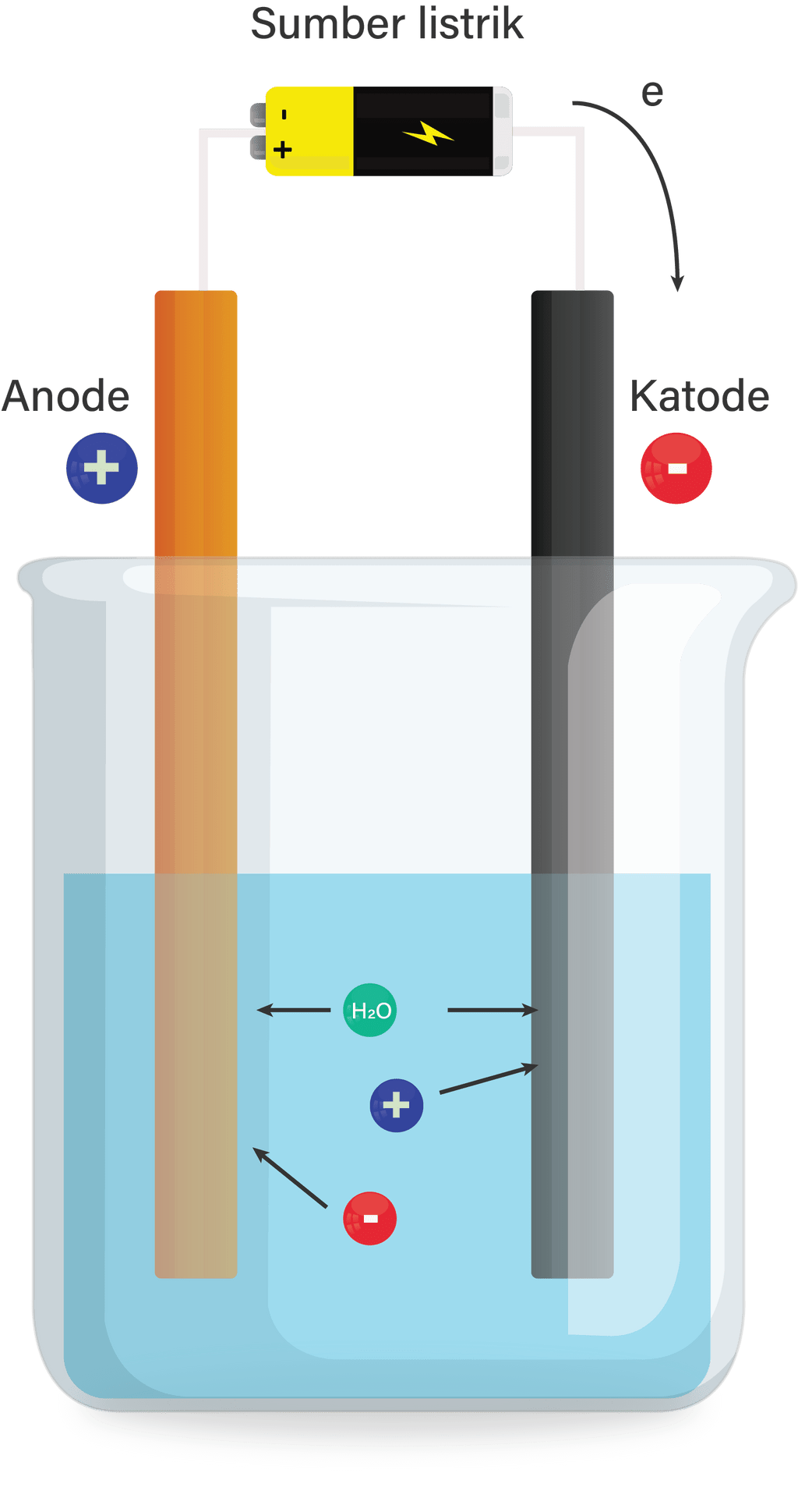
Prioritas reaksi reduksi di katode: I. kation, II. air.
Jika kation lebih mudah tereduksi daripada air, maka kation yang tereduksi. Jika sebaliknya, maka molekul air yang tereduksi.
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
4
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia
















