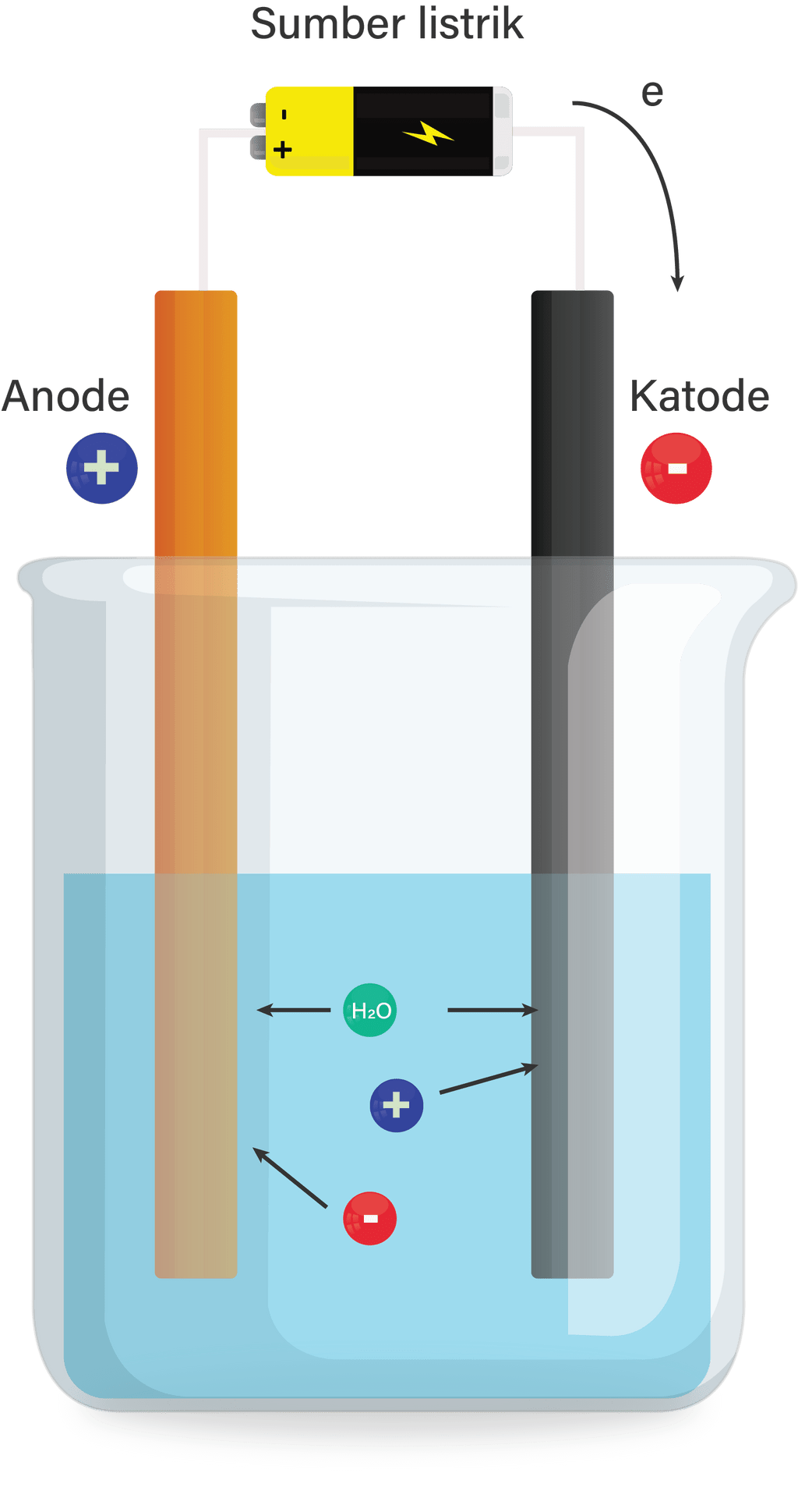
Berdasarkan gambar pada soal, larutan elektrolit menjadi ion positif (kation) dan ion negatif (anion), ketika sumber listrik dinyalakan, ion-ion negatif akan mendekati kutub positif (anode). Apabila potensial reduksi air lebih besar daripada potensial reduksi ion negatif, maka ion akan teroksidasi di anode, jika sebaliknya, maka air teroksidasi, dan elektron yang dilepaskan bergerak ke katode sehingga terjadi reaksi reduksi di katode.
Elektrode noninert (selain C, Pt, Au) merupakan elektrode yang reaktif dan memiliki nilai potensial reduksi yang kecil sehingga mengalami reaksi oksidasi. Sedangkan elektrode inert seperti C, Pt, dan Au sama sekali tidak bereaksi pada sel elektrolisis, sehingga reaksi oksidasi pada anode tergantung pada anion elektrolit.
Spesi yang mengalami oksidasi di anode berupa spesi yang mempunyai potensial elektrode lebih negatif (lebih kecil). Perhatikan! Reaksi reduksi air tidak berkebalikan dengan reaksi oksidasi air.
Reduksi: 2H2O+2e−→H2+2OH− E∘=−0,83 VOksidasi: 2H2O→4H++O2+4e− E∘=−1,23 V
Dapat dilihat bahwa reaksi oksidasi air merupakan kebalikan dari reaksi reduksi oksigen, oleh sebab itu, nilai potensial reduksi yang diperhatikan adalah potensial reduksi oksigen. Jika dibandingkan dengan potensial reduksi anion sisa asam oksi, misalnya SO42−, reaksi yang mungkin terjadi di anode adalah:
2SO42−(aq)→S2O82−(aq)+2e−2H2O→4H+(aq)+O2(g)+2e−
dan reaksi setengah sel (reduksi) dan nilai potensial reduksi yang dapat kita temui di tabel adalah sebagai berikut:
S2O82−(aq)+2e−→2SO42−(aq) E∘=+2,01 VO2(g)+4H+(aq)+4e−→2H2O E∘=+1,23 V
Terlihat nilai potensial reduksi S2O82− lebih besar (lebih mudah tereduksi) daripada oksigen karena nilai potensial reduksinya lebih besar. Sebaliknya, SO42− tentu lebih sulit untuk teroksidasi. Dengan kata lain, spesi dengan nilai potensial reduksi lebih kecil akan lebih mudah mengalami reaksi oksidasi. Anion-anion sisa asam oksi lain seperti NO3−, CO32−, MnO4−, dan ClO4− termasuk anion yang sangat sukar teroksidasi. Jika diperhatikan dari bilangan oksidasi atom pusatnya,
- biloks N dalam NO3− adalah +5
- biloks C dalam CO32− adalah +4
- biloks Mn dalam MnO4− adalah +7
- biloks Cl dalam ClO4− adalah +7
merupakan bilangan oksidasi maksimum yang dimiliki unsur-unsur tersebut, yang artinya tidak dapat dioksidasi lagi.
Demikian pula jika anionnya berupa anion halida, seperti ion Br−, reaksi reduksi dan nilai potensial reduksinya adalah sebagai berikut:

Data tersebut menunjukkan bahwa reaksi reduksi oksigen lebih mudah terjadi dibandingkan reaksi reduksi ion Br−, artinya ion Br− akan mengalami reaksi oksidasi.
Namun demikian, ada beberapa keadaan dimana nilai potensial reduksi standar tidak selalu dapat memprediksi produk elektrolisis dengan benar, seperti anion Cl− dengan nilai E∘ = +1,36 V. Jika dibandingkan dengan potensial reduksi oksigen (1,23 V), maka seharusnya air yang akan mengalami reaksi oksidasi, ternyata secara eksperimen Cl2 dihasilkan pada anoda (hasil reaksi oksidasi Cl−). Beberapa faktor seperti konsentrasi, keadaan yang tidak begitu standar, permukaan elektroda, dapat mengubah potensial sel. Oleh sebab itu berdasarkan eksperimen diperoleh bahwa anion-anion halogen lebih mudah teroksidasi daripada molekul air pada anode sel elektrolisis.
Sehingga, reaksi-reaksi pada anode sel elektrolisis mengikuti prioritas berikut.
- Anode inert (C, Pt, Au): elektrode yang tidak bereaksi.
- Sisa asam oksi (SO42−, NO3−, PO43−, dan CO32−) memiliki nilai E∘ > daripada E∘ air, maka air akan teroksidasi.
- Anion lain (OH−, O2−, Br−, Cl−) memiliki nilai E∘ < daripada E∘ air, maka anion yang teroksidasi.
- Anode noninert: elektrode yang reaktif.
Contoh anion yang bukan inert Zn, Fe, Co (selain C, Pt, Au) memiliki E∘ < daripada E∘ air, maka elektrode akan teroksidasi.
Jadi, prioritas tersebut benar, reaksi oksidasi pada anode sel elektrolisis memperhatikan jenis elektrode (anode) terlebih dahulu, jika anode tidak inert, maka anode teroksidasi, dan jika anode inert, perhatikan jenis anionnya.