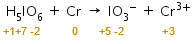Penyetaraan reaksi redoks dengan metode biloks dalam suasana asam adalah sebagai berikut.
Langkah 1: menghitung biloks setiap unsur.
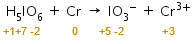
Langkah 2: mengidentifikasi unsur yang mengalami perubahan biloks.
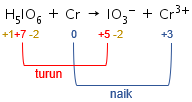
Langkah 3: menyamakan jumlah unsur yang mengalami perubahan biloks, yaitu unsur I dan Cr.
Pada reaksi ini, jumlah atom I dan Cr pada ruas kiri dan kanan sudah sama, yaitu 1 sehingga tidak ada perubahan koefisien.
Langkah 4: menghitung total biloks unsur yang mengalami perubahan biloks dengan cara dikalikan dengan indeks atau koefisien unsur.
Jumlah unsur I dan Cr pada ruas kiri dan kanan adalah 1, maka biloks unsur I dan Cr dikalikan 1.

Langkah 5: menghitung total perubahan biloks pada reaksi.
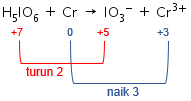
Langkah 6: menyamakan total perubahan biloks pada reaksi.
Kenaikan biloks unsur Cr adalah 3, sedangkan penurunan biloks unsur I adalah 2. Agar total perubahan biloksnya sama, maka cari kelipatan antara 2 dan 3, yaitu 6. Dengan demikian, kenaikan biloks unsur Cr dikalikan 2 dan penurunan biloks unsur I dikalikan 2.
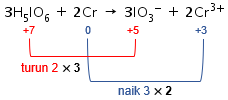
Angka faktor pengali 2 menjadi pengali koefisien dari zat yang mengandung unsur Cr, sedangkan angka faktor pengali 3 menjadi pengali koefisien dari zat yang mengandung unsur I.
Langkah 7: menyamakan jumlah muatan dengan menambah ion  pada ruas yang muatannya lebih kecil.
pada ruas yang muatannya lebih kecil.
Muatan pada ruas kiri adalah 0, sedangkan muatan pada ruas kanan adalah +3. Oleh karena itu, 3 ion  ditambahkan pada ruas kiri sehingga persamaan reaksinya menjadi
ditambahkan pada ruas kiri sehingga persamaan reaksinya menjadi

Langkah 8: menyamakan jumlah oksigen dengan menambahkan  pada ruas yang kekurangan oksigen.
pada ruas yang kekurangan oksigen.
Terdapat 18 atom O pada ruas kiri dan 9 atom O pada ruas kanan. Artinya, di ruas kanan kurang 9 atom O sehingga perlu menambahkan 9  . Persamaan reaksinya menjadi
. Persamaan reaksinya menjadi

Langkah 9: memeriksa kembali reaksi setara.

Selanjutnya, mol  yang terbentuk dihitung dengan menggunakan perbandingan koefisien.
yang terbentuk dihitung dengan menggunakan perbandingan koefisien.
n H2On H2On H2O===koef H5IO6 koef H2O×n H5IO639×3 mol9 mol
Jadi, jawaban yang tepat adalah B.