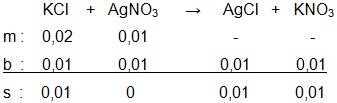Iklan
Pertanyaan
100 mL larutan KCl 0,2 M direaksikan dengan 200 mL larutan AgNO 3 0,05 M . Persamaan reaksinya: KCl ( a q ) + AgNO 3 ( a q ) → AgCl ( s ) + KNO 3 ( a q ) Berapakah massa AgCl yang dihasilkan ( A r Ag = 108, Cl = 35,5)?
100 mL larutan KCl 0,2 M direaksikan dengan 200 mL larutan 0,05 M. Persamaan reaksinya:
Berapakah massa AgCl yang dihasilkan ( Ag = 108, Cl = 35,5)?
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
6
4.5 (4 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia