Muhammad Y
31 Juli 2025 13:55
Iklan
Muhammad Y
31 Juli 2025 13:55
Pertanyaan
3. Silikon tetraklorida (SiCl4) dibuat dengan memanaskan Si dalam gas klorin menurut reaksi berikut: Si(s) + 2Cl2(g) → SiCl4(1) Jika dalam reaksi dihasilkan sebanyak 0,507 mol, maka berapakah volume (L) gas klorin yang digunakan pada suhu 0°C dan tekanan 1 atm?
3. Silikon tetraklorida (SiCl4) dibuat dengan memanaskan Si dalam gas klorin menurut reaksi berikut:
Si(s) + 2Cl2(g) → SiCl4(1) Jika dalam reaksi dihasilkan sebanyak 0,507 mol, maka berapakah volume (L) gas klorin yang digunakan pada suhu 0°C dan tekanan 1 atm?
2
2
Iklan
Patrick H
01 Agustus 2025 08:20
<p>Kita punya persamaan reaksi produksi SiCl<sub>4</sub> sebagai berikut.</p><p>Si(<i>s</i>) + 2Cl<sub>2</sub>(<i>g</i>) → SiCl<sub>4</sub>(<i>l</i>)</p><p>Perhatikan bahwa perbandingan koefisien mol pada persamaan reaksi tersebut adalah:</p><p>1 mol Si : 2 mol Cl<sub>2</sub> : 1 mol SiCl<sub>4</sub></p><p> </p><p>Maka, jika dalam suatu reaksi dihasilkan SiCl<sub>4</sub> sebanyak 0,507 mol, maka reaksi tersebut perlu menggunakan gas klorin sebanyak 2 × 0,507 mol = 1,014 mol.</p><p> </p><p>Kondisi suhu 0°C (273 K) dan tekanan 1 atm disebut juga dengan kondisi STP (<i>Standard Temperature and Pressure</i>/Suhu dan Tekanan Standar). Pada kondisi tersebut, gas ideal memiliki volume molar 22,4 L/mol, yang berarti tiap mol gas memiliki volume 22,4 L.</p><p>Maka, volume 1,014 mol gas Cl<sub>2</sub> pada kondisi STP adalah 1,014 mol × 22,4 L/mol = 22,7136 L ≈ <strong>22,7 L</strong>.</p>
Kita punya persamaan reaksi produksi SiCl4 sebagai berikut.
Si(s) + 2Cl2(g) → SiCl4(l)
Perhatikan bahwa perbandingan koefisien mol pada persamaan reaksi tersebut adalah:
1 mol Si : 2 mol Cl2 : 1 mol SiCl4
Maka, jika dalam suatu reaksi dihasilkan SiCl4 sebanyak 0,507 mol, maka reaksi tersebut perlu menggunakan gas klorin sebanyak 2 × 0,507 mol = 1,014 mol.
Kondisi suhu 0°C (273 K) dan tekanan 1 atm disebut juga dengan kondisi STP (Standard Temperature and Pressure/Suhu dan Tekanan Standar). Pada kondisi tersebut, gas ideal memiliki volume molar 22,4 L/mol, yang berarti tiap mol gas memiliki volume 22,4 L.
Maka, volume 1,014 mol gas Cl2 pada kondisi STP adalah 1,014 mol × 22,4 L/mol = 22,7136 L ≈ 22,7 L.
· 0.0 (0)
Iklan
Isma R
02 Agustus 2025 13:33
<p> </p><p>Jadi jawbannya 22,72 L</p>
Jadi jawbannya 22,72 L
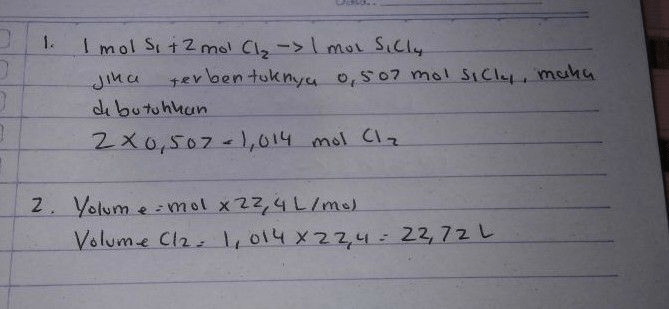
· 0.0 (0)
Mau jawaban yang terverifikasi?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



