Iklan
Pertanyaan
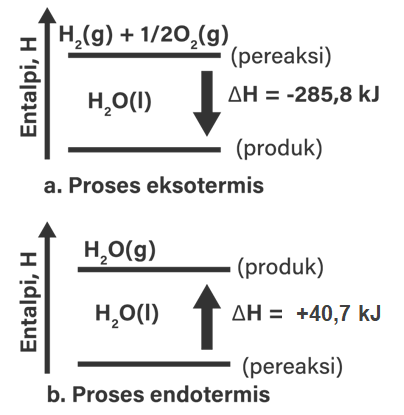
Untuk setiap proses berikut, tentukan tanda nilai △ H , apakah reaksi berlangsung secara eksotermis atau endotermis, dan gambarkan diagram entalpinya. (a) H 2 ( g ) + 2 1 O 2 ( g ) → H 2 O ( l ) + 285 , 8 kJ (b) 40 , 7 kJ + H 2 O ( l ) → H 2 O ( g )
Untuk setiap proses berikut, tentukan tanda nilai , apakah reaksi berlangsung secara eksotermis atau endotermis, dan gambarkan diagram entalpinya.
(a)
(b)
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
2
4.5 (4 rating)
SR
Syifa Ramadhani
Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia