Iklan
Pertanyaan
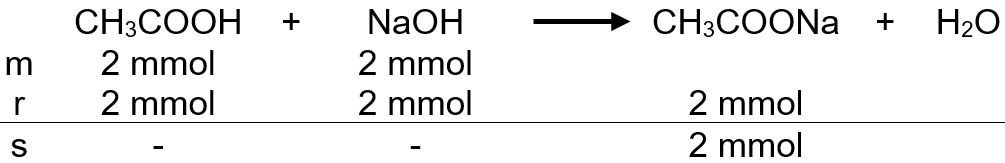
Untuk menentukan konsentrasi larutan CH 3 COOH , diambil 10 mL larutan tersebut kemudian dititrasi dengan larutan NaOH 0,1 M. Ternyata, titik akhir titrasi terjadi pada saat volume NaOH 20 mL. Tentukan: b. pH pada titik ekivalen, dan
Untuk menentukan konsentrasi larutan diambil 10 mL larutan tersebut kemudian dititrasi dengan larutan NaOH 0,1 M. Ternyata, titik akhir titrasi terjadi pada saat volume NaOH 20 mL. Tentukan:
b. pH pada titik ekivalen, dan
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
5
5.0 (3 rating)
GE
Gabriella Editha
Pembahasan lengkap banget Mudah dimengerti Bantu banget Makasih ❤️
EG
Elizabeth Gita
Ini yang aku cari!
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia