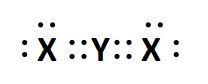Iklan
Pertanyaan
Unsur X memiliki konfigurasi elektron: 1s 2 2s 2 2p 6 3s 2 3p 4 dan unsur Y memiliki konfigurasi elektron: 1s 2 2s 2 2p 2 . Bentuk molekul yang terjadi jika kedua unsur tersebut berikatan menurut aturan oktet adalah ....
Unsur X memiliki konfigurasi elektron: 1s2 2s2 2p6 3s2 3p4 dan unsur Y memiliki konfigurasi elektron: 1s2 2s2 2p2 .
Bentuk molekul yang terjadi jika kedua unsur tersebut berikatan menurut aturan oktet adalah ....
linear
bentuk V
segiempat datar
segitiga piramida
segitiga bipiramida
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
5
4.4 (5 rating)
BM
Bilqis Madani
Pembahasan lengkap banget
HS
Hana Syakira
Pembahasan tidak lengkap
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia