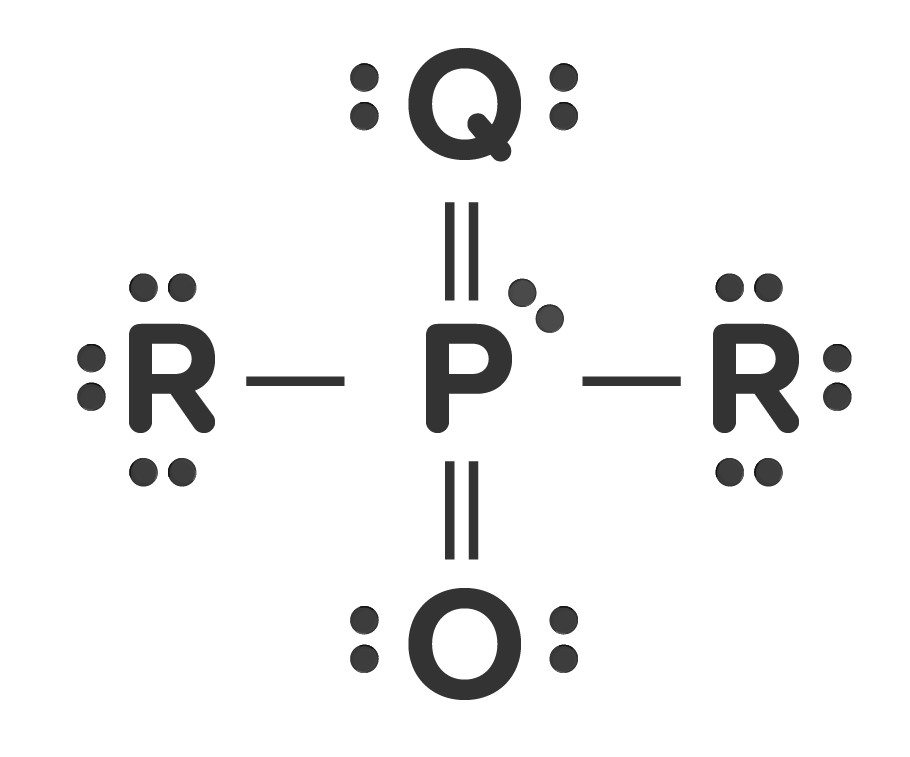Iklan
Pertanyaan
Unsur P terletak pada golongan VIIIA dan periode 5, sedangkan unsur Q dan R secara berurutan memiliki nomor atom 8 dan 9. Ketiga unsur tersebut akan membentuk senyawa PQ 2 R 2 . Tipe dan bentuk molekul dari senyawa tersebut adalah ....
Unsur P terletak pada golongan VIIIA dan periode 5, sedangkan unsur Q dan R secara berurutan memiliki nomor atom 8 dan 9. Ketiga unsur tersebut akan membentuk senyawa . Tipe dan bentuk molekul dari senyawa tersebut adalah ....
dan tetrahedral terdistorsi
dan tetrahedral
dan segi empat piramida
dan segitiga planar
dan segi empat planar
Iklan
MB
M. Banyu
Master Teacher
Jawaban terverifikasi
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia