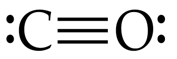Iklan
Pertanyaan
Karbon monoksida adalah polutan udara yang berbahaya bagi tubuh. Gas karbon monoksida dihasilkan dari pembakaran tidak sempurna senyawakarbon. Gas ini dapat berikatan dengan hemoglobin dalam tubuhsehingga pengikatan oksigen oleh darah menjadi terganggu. Muatan formal atom C dan O dalam senyawa karbon monoksida secara berurutan adalah ....(Nomor atom C = 6 dan O = 8)
Karbon monoksida adalah polutan udara yang berbahaya bagi tubuh. Gas karbon monoksida dihasilkan dari pembakaran tidak sempurna senyawa karbon. Gas ini dapat berikatan dengan hemoglobin dalam tubuh sehingga pengikatan oksigen oleh darah menjadi terganggu. Muatan formal atom C dan O dalam senyawa karbon monoksida secara berurutan adalah .... (Nomor atom C = 6 dan O = 8)
Iklan
M. Rizki
Master Teacher
1
2.0 (4 rating)
Shofa Nur Radhiya
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Bantu banget Makasih ❤️
Alya Silviana Mahira
Jawaban tidak sesuai
LANCE
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia