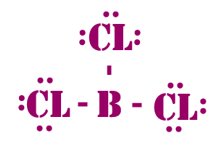Iklan
Pertanyaan
Unsur B dan X memiliki konfigurasi elektron sebagai berikut: B = 1s 2 2s 2 2p 1 X = 1s 2 2s 2 2p 5 Jika kedua unsur berikatan, maka bentuk molekul dari senyawa tersebut adalah ….
Unsur B dan X memiliki konfigurasi elektron sebagai berikut:
B = 1s22s22p1
X = 1s22s22p5
Jika kedua unsur berikatan, maka bentuk molekul dari senyawa tersebut adalah ….
linear
segitiga datar
tetrahedral
segitiga piramida
bentuk V
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
1
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia