Iklan
Pertanyaan
Informasi berikut digunakan untuk menjawab soal nomor 1 dan 2.
Perhatikan senyawa berikut!
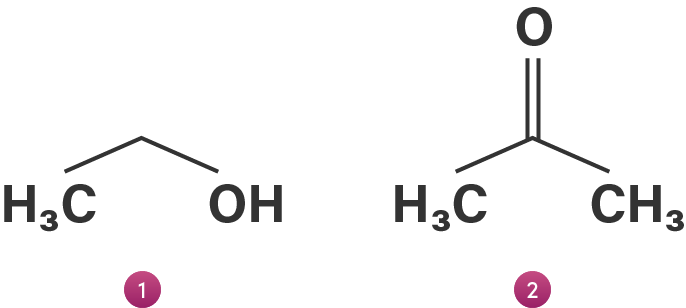
Diketahui
Titik didih senyawa (1) lebih besar dari senyawa (2). Hal ini disebabkan oleh ....
Titik didih senyawa (1) lebih besar dari senyawa (2). Hal ini disebabkan oleh ....
senyawa (2) memiliki ikatan hidrogen lebih lemah daripada senyawa (1)
senyawa (1) memiliki gaya dispersi london lebih besar daripada senyawa (2)
senyawa (2) memiliki interaksi dipol-dipollebih lemah daripada senyawa (1)
senyawa (1) memiliki struktur yang lebih pendek daripada senyawa (2)
senyawa (1) memiliki ikatan hidrogen sedangkan senyawa (2) tidak
Iklan
Q. 'Ainillana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
1
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















