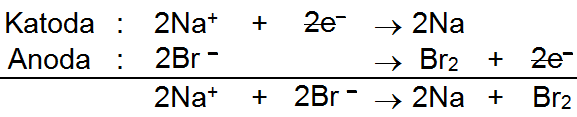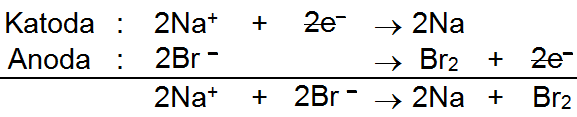Dalam sel elektrolisis, arus listrik digunakan untuk menghasilkan reaksi kimia (reaksi redoks). Reaksi redoks yang terjadi berlangsung secara tidak spontan. Proses reaksi ini terbentuk karena adanya aliran listrik yang berasal dari rangkaian luar. Dalam membuat reaksi elektrolisis, ion positif tidak selalu mengalami reduksi pada katode dan ion negatif juga tidak selalu mengalami reaksi oksidasi pada anode. Hal ini tergantung pada kecenderungan suatu ion untuk mengalami reaksi reduksi atau oksidasi.
Pada soal di atas, leburan senyawa NaBr dielektrolisis dengan elektrode C. Elektroda C (karbon) termasuk elektroda yang bersifat inert, atau tidak terlibat dalam reaksi elektrolisis dan hanya menyediakan permukaannya untuk terjadinya reaksi. Senyawa NaBr yang dielektrolisis berwujud leburan atau lelehan, sehingga tidak terdapat air dan tidak terjadi persaingan antara kation dan anion dengan molekul air untuk mengalami reaksi oksidasi ataupun reduksi. Pada senyawa yang dielektrolisis berwujud lelehan atau leburan, kation golongan utama atau golongan transisi langsung direduksi.
Sebelum dibuat persamaan reaksi pada anoda dan katodanya, terlebih dahulu senyawa NaBr dibuat reaksi ionisasinya sebagai berikut.
NaBr→Na++Br−
Reaksi yang terjadi pada anoda dan katoda dalam elektrolisis leburan senyawa NaBr adalah sebagai berikut.
Katoda = Na++e−→Na
Anoda = 2Br−→Br2+2e−
![]()

Untuk menyamakan jumlah elektron yang terlibat, maka persamaan reaksi pada katoda harus dikalikan 2 agar di kedua reaksi jumlah elektron yang terlibat berjumlah 2. Selanjutnya, persamaan reaksinya menjadi sebagai berikut.
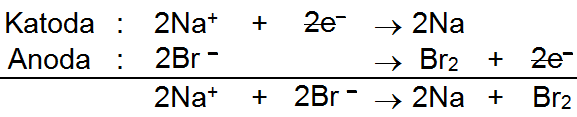
Dengan demikian, reaksi yang terjadi di anode dan di katode pada elektrolisis leburan NaBr dengan elektrode C adalah sebagai berikut.