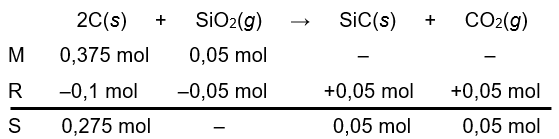Iklan
Pertanyaan
Silikon karbida atau karborundum dapat diperoleh dengan mereaksikan SiO 2 ( A r Si = 28, O = 16) dengan karbon ( A r C = 12) pada temperatur tinggimenurut reaksi: 2 C ( s ) + SiO 2 ( s ) → SiC ( s ) + CO 2 ( g ) Jika 4,5 g karbon direaksikan dengan 3,0 g menghasilkan 1,5 g karborundum, persentase hasil reaksi tersebut adalah .... (SBMPTN 2015)
Silikon karbida atau karborundum dapat diperoleh dengan mereaksikan ( Si = 28, O = 16) dengan karbon ( C = 12) pada temperatur tinggi menurut reaksi:
Jika 4,5 g karbon direaksikan dengan 3,0 g menghasilkan 1,5 g karborundum, persentase hasil reaksi tersebut adalah ....
(SBMPTN 2015)
20%
38%
60%
75%
90%
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
1
5.0 (3 rating)
0
000000000000000000000000c6648aad558d82ef3a16184dec38e7aa0dc9eaecff8a77c0340d80e359ac6cb86e07bf39
Ini yang aku cari!
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia