Iklan
Pertanyaan
Seorang siswa melakukan titrasi larutan NaOH 0,1 M dengan larutan HCI diperoleh data sebagai berikut: Berdasarkan data di atas, maka harga pH larutan HCl adalah ...
Seorang siswa melakukan titrasi larutan NaOH 0,1 M dengan larutan HCI diperoleh data sebagai berikut:
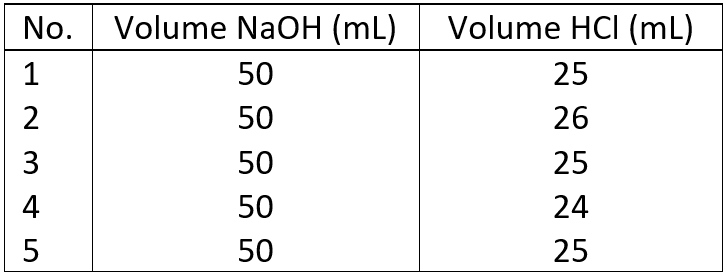
Berdasarkan data di atas, maka harga pH larutan HCl adalah ...
1 - log 2
1 + log 2
2 + log 2
13 - log 2
13 + log 2
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
3
4.3 (8 rating)
a
achra
Makasih ❤️
SM
Siti Maesaroh
Makasih ❤️
z
zahra
Pembahasan lengkap banget
NB
Nadia Bilqis Bestari
Pembahasan tidak menjawab soal
SF
Sherleen Felicia
Pembahasan tidak menjawab soal Pembahasan tidak lengkap
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















