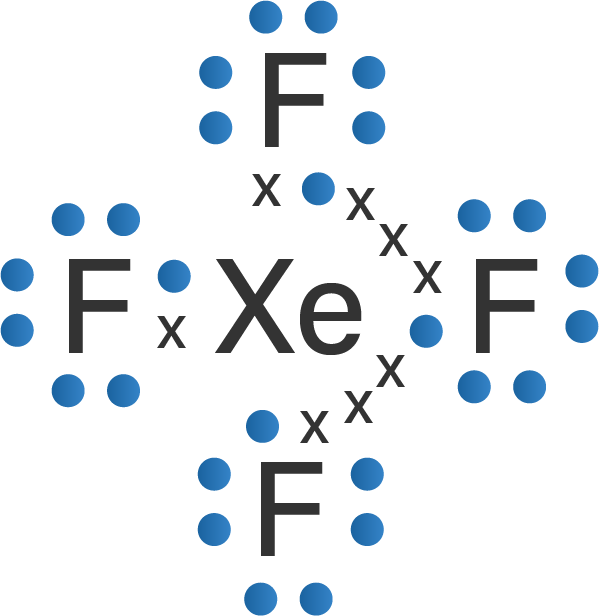Bentuk molekul menentukan sifat kepolaran senyawa kovalen. Jika di dalam molekul terdapat pemisahan muatan maka kerapatan elektron dalam molekul tidak merata sehingga molekul bersifat polar. Sebaliknya, jika kerapatan elektron tersebar merata maka molekul bersifat nonpolar. Senyawa kovalen ada yang polar dan ada yang nonpolar. Senyawa kovalen bersifat nonpolar jika molekulnya berbentuk simetris. Hal itu terjadi karena muatan positif berimpit dengan muatan negatif. Senyawa kovalen akan bersifat polar jika pada atom pusat dari molekul senyawa tersebut terdapat pasangan elektron bebas sehingga bentuk molekulnya menjadi tidak simetris.
Untuk dapat menjawab soal di atas, maka terlebih dahulu perlu dibuat konfigurasi elektron dari unsur 6C, 16S, dan 54Xe. Konfigurasi elektron dari ketiga unsur tersebut adalah sebagai berikut.
6C16S54Xe===1s2 2s2 2p2[10Ne] 3s2 3p4[36Kr] 5s2 4d10 5p6
Berdasarkan konfigurasi elektron unsur C, S, dan Xe di atas, diketahui bahwa atom C memiliki 4 buah elektron valensi, atom S memiliki 6 elektron valensi dan atom Xe memiliki 8 elektron valensi. Unsur C, S, dan Xe dapat membentuk senyawa dengan atom fluor (F), seperti CF4, SF4, SF6, XeF2 dan XeF4. Struktur Lewis dari senyawa CF4, SF4, SF6, XeF2 dan XeF4 adalah sebagai berikut.

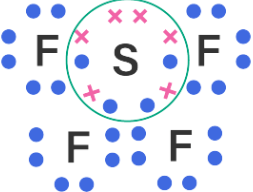
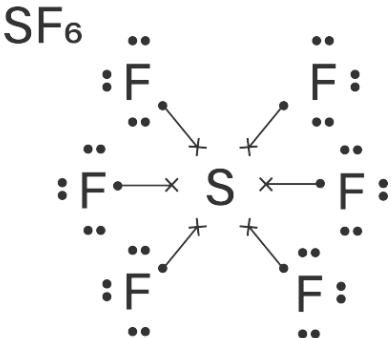

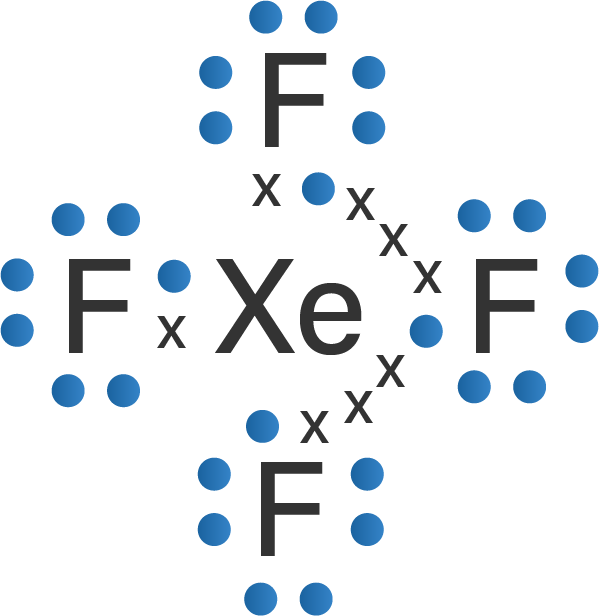
Berdasarkan struktur Lewis senyawa CF4, SF4, SF6, XeF2 dan XeF4 di atas, diketahui bahwa pada senyawa SF4, XeF2 dan XeF4 masih memiliki pasangan elektron bebas (PEB) di atom pusatnya. Senyawa SF4 memiliki 1 buah PEB pada atom S, senyawa XeF2 memiliki 3 buah PEB pada atom Xe, dan senyawa XeF4 memiliki 2 buah PEB pada atom Xe. Senyawa CF4 dan SF6 tidak memiliki PEB pada atom pusatnya, maka bentuk molekul senyawanya akan berbentuk simetris sehingga bersifat nonpolar.
Senyawa-senyawa yang memiliki PEB dirumuskan tipe molekulnya dengan notasi A, X, E, dengan A sebagai atom pusat, X sebagai pasangan elektron berikatan (PEI), dan E merupakan pasangan elektron bebas (PEB). Tipe molekul dari senyawa SF4 yang memiliki 1 buah PEB dan 4 buah PEI adalah AX4E dan memiliki bentuk molekul tetrahedral terdistorsi atau bentuk jungkat jungkit. Tipe molekul dari senyawa XeF2 yang memiliki 3 buah PEB dan 2 buah PEI adalah AX2E3 dan memiliki bentuk molekul linier. Tipe molekul dari senyawa XeF4 yang memiliki 2 buah PEB dan 4 buah PEI adalah AX4E2 dan memiliki bentuk molekul segi empat planar. Dari ketiga bentuk molekul senyawa SF4, XeF2 dan XeF4, molekul yang bersifat polar adalah SF4 yang memiliki bentuk molekul tetrahedral terdistorsi atau bentuk jungkat jungkit.
Dengan demikian, maka senyawa florida yang terbentuk dari atom 6C, 16S, atau 54Xe yang bersifat polar adalah SF4.
Jadi, jawaban yang tepat adalah B.