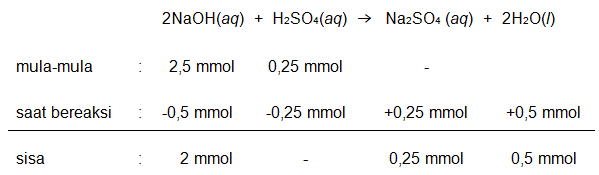Iklan
Pertanyaan
Sebanyak 50 mL larutan H 2 SO 4 0,005 M dicampur dengan 50 mL larutan NaOH 0,05 M. Hitung pH larutan tersebut sebelum dan sesudah dicampurkan.
Sebanyak 50 mL larutan 0,005 M dicampur dengan 50 mL larutan 0,05 M. Hitung pH larutan tersebut sebelum dan sesudah dicampurkan.
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
10
4.8 (15 rating)
AF
Anya Flora
Pembahasan lengkap banget Ini yang aku cari! Makasih ❤️ Mudah dimengerti Bantu banget
ZS
Zahratul Shyita
Pembahasan lengkap banget Makasih ❤️
0D
09. Dwi Miranda
Terima kasih kak
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia