Iklan
Pertanyaan
Sebanyak 20 mL larutan KOH 0,1 M ditetesi dengan larutan CH 3 COOH 0,1 M. a. Perkirakan pH awal larutan KOH. b. Secara teori, berapa mL larutan yang diperlukan untuk mecapai titik ekuivalen? c. Berapakah kira-kira pH pada titik ekuivalen? d. Gambarkan (sketsa) kurva titrasinya. e. Tentukan indikator yang dapat digunakan. Bagaimanakah perubahan warnanya pada titik akhir titrasi? ( K a CH 3 COOH = 1 , 8 × 1 0 − 5 )
Sebanyak 20 mL larutan KOH 0,1 M ditetesi dengan larutan 0,1 M.
a. Perkirakan pH awal larutan KOH.
b. Secara teori, berapa mL larutan yang diperlukan untuk mecapai titik ekuivalen?
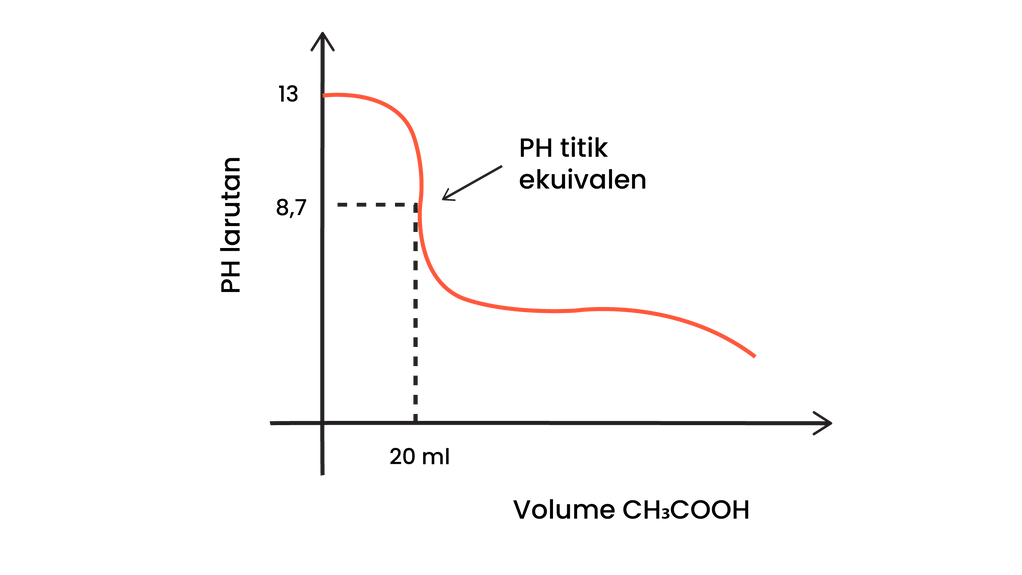
c. Berapakah kira-kira pH pada titik ekuivalen?
d. Gambarkan (sketsa) kurva titrasinya.
e. Tentukan indikator yang dapat digunakan. Bagaimanakah perubahan warnanya pada titik akhir titrasi?
Iklan
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
4
4.5 (12 rating)
INDANA LAZULFA
Makasih ❤️
Fania Natasya Ramadhani
Bantu banget
Angelina Alexa
Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia