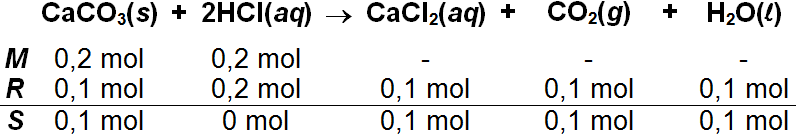Iklan
Pertanyaan
Sebanyak 20 gram CaCO 3 dilarutkan dalam 1 liter larutan asam klorida 0,2 M menurut persamaan reaksi: CaCO 3 ( s ) + 2 HCl ( a q ) → CaCl 2 ( a q ) + CO 2 ( g ) + H 2 O ( l ) b. Berapa liter volume gas karbon dioksida yang dihasilkan bila diukur pada suhu dan tekanan yang sama pada saat 2 liter gas NO ( A r N = 14 dan O = 16) massanya 1,2 gram?
Sebanyak 20 gram dilarutkan dalam 1 liter larutan asam klorida 0,2 M menurut persamaan reaksi:
b. Berapa liter volume gas karbon dioksida yang dihasilkan bila diukur pada suhu dan tekanan yang sama pada saat 2 liter gas ( N = 14 dan O = 16) massanya 1,2 gram?
Iklan
NA
N. Agnia
Master Teacher
Mahasiswa/Alumni Institut Pertanian Bogor
Jawaban terverifikasi
27
4.6 (8 rating)
a
ayaaa
Pembahasan lengkap banget
Ik
Intan kirana dwi prabowo putri
Ini yang aku cari!
AA
Aulia Amalia
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia