Iklan
Pertanyaan
Reaksi X + 2 Y → Z dipelajari kinetikanya dan diperoleh data sebagai berikut. Pernyataan yang benar mengenai reaksi di atas adalah ... Nilai x adalah 1 , 44 M / s Orde reaksi dapat ditentukan secara langsung dari koefisien reaksi Reaksi tersebut memiliki konstanta laju sebesar 16 M − 1 s − 1 Orde terhadap Y adalah 2
Reaksi dipelajari kinetikanya dan diperoleh data sebagai berikut.
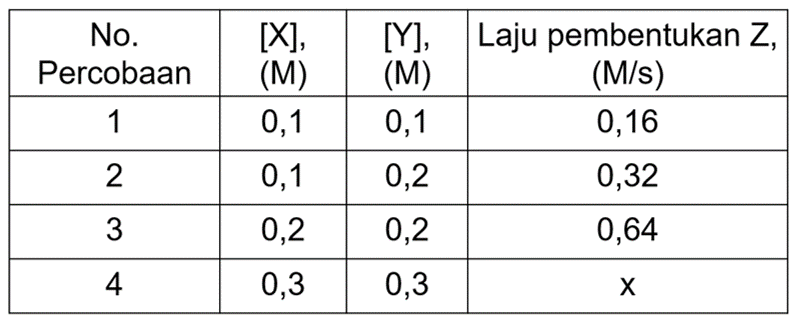
Pernyataan yang benar mengenai reaksi di atas adalah ...
- Nilai adalah
- Orde reaksi dapat ditentukan secara langsung dari koefisien reaksi
- Reaksi tersebut memiliki konstanta laju sebesar
- Orde terhadap adalah
1, 2, dan 3 SAJA yang benar.
1 dan 3 SAJA yang benar.
2 dan 4 SAJA yang benar.
HANYA 4 yang benar.
SEMUA pilihan benar.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















