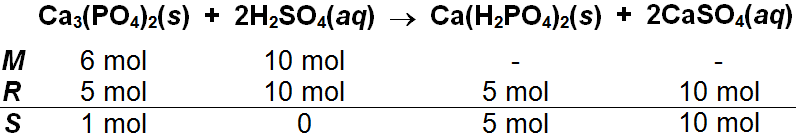Iklan
Pertanyaan
Pupuk superfosfat ( Ca ( H 2 PO 4 ) 2 ) dibuat dengan mereaksikan kalsium fosfat dengan larutan asam sulfat. Persamaan reaksinya: Ca 3 ( PO 4 ) 2 + 2 H 2 SO 4 → Ca ( H 2 PO 4 ) 2 ( s ) + 2 CaSO 4 ( a q ) Tentukan massa pupuk superfosfat yang terbentuk jika direaksikan 1.860 gram Ca 3 ( PO 4 ) 2 dengan 10 liter H 2 SO 4 1 M? ( A r Ca = 40, H = 1, P = 31, dan O = 32)
Pupuk superfosfat dibuat dengan mereaksikan kalsium fosfat dengan larutan asam sulfat. Persamaan reaksinya:
Tentukan massa pupuk superfosfat yang terbentuk jika direaksikan 1.860 gram dengan 10 liter 1 M? ( Ca = 40, H = 1, P = 31, dan O = 32)
Iklan
AK
A. Kusbardini
Master Teacher
Mahasiswa/Alumni UIN Syarif Hidayatullah Jakarta
Jawaban terverifikasi
8
4.6 (6 rating)
a
ayaaa
Pembahasan lengkap banget Mudah dimengerti
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia