Iklan
Pertanyaan
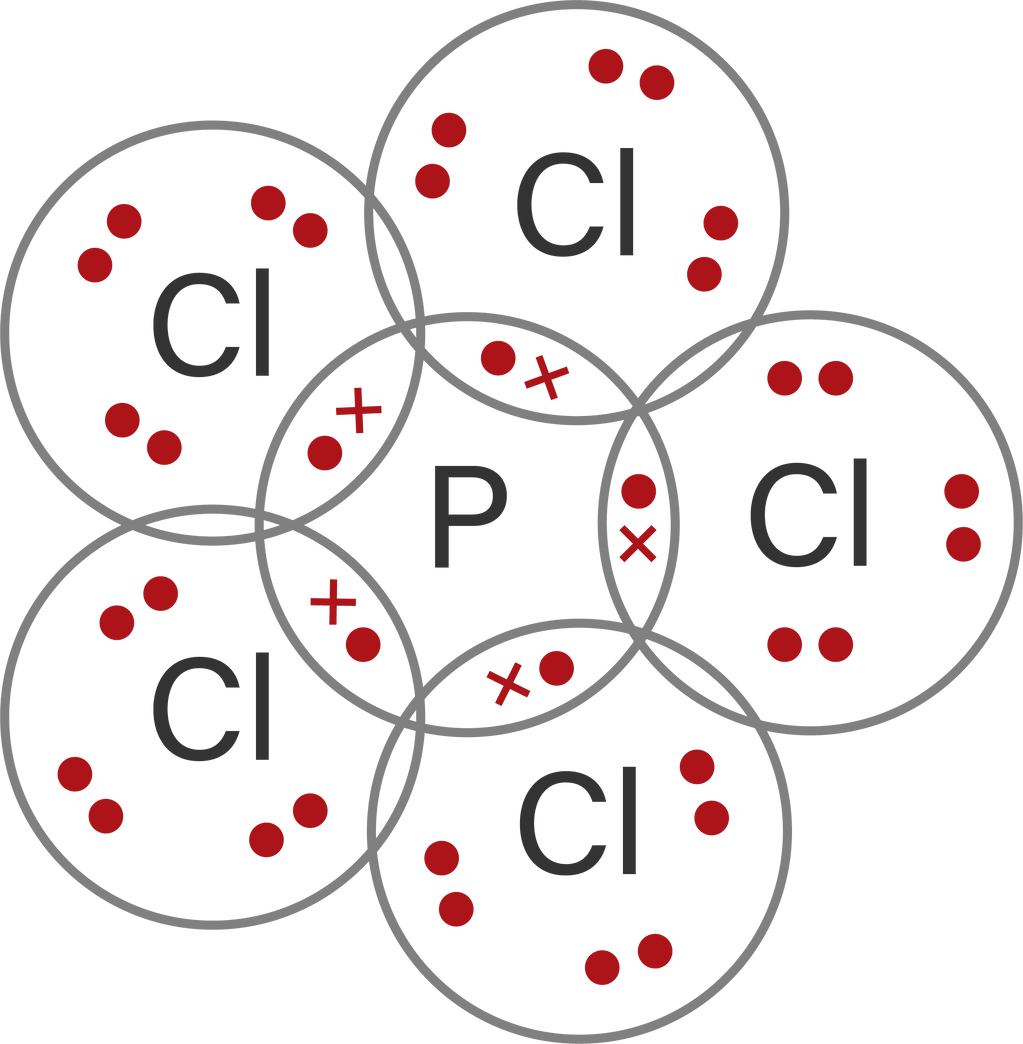
Perhatikan senyawa kovalen berikut. CH 4 PCl 5 NH 3 CHCl 3 H 2 O Jika diketahui nomor atom H = 1, C = 6, N = 7, O = 8, P = 15, Cl = 17, senyawa yang tidak mengikuti aturan oktet adalah....
Perhatikan senyawa kovalen berikut.
Jika diketahui nomor atom H = 1, C = 6, N = 7, O = 8, P = 15, Cl = 17, senyawa yang tidak mengikuti aturan oktet adalah ....
(1)
(2)
(3)
(4)
(5)
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
2
4.3 (6 rating)
bn
baiq nadila mustika
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia