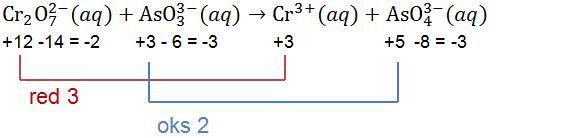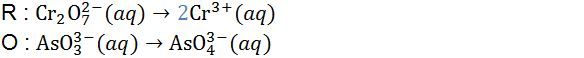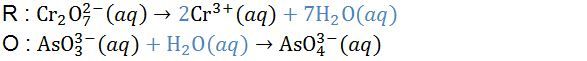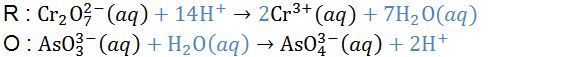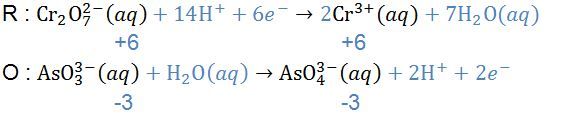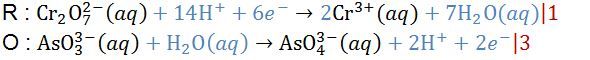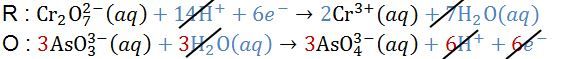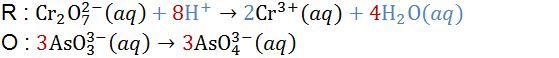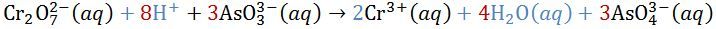Iklan
Pertanyaan
Perhatikan reaksi redoks berikut! Cr 2 O 7 2 − ( a q ) + AsO 3 3 − ( a q ) → Cr 3 + ( a q ) + AsO 4 3 − ( a q ) Setelah reaksi disetarakan, perbandingan antara mol ion Cr 2 O 7 2 − dengan AsO 4 3 − dalam reaksi tersebut adalah ....
Perhatikan reaksi redoks berikut!
Setelah reaksi disetarakan, perbandingan antara mol ion dengan dalam reaksi tersebut adalah ....
1 : 3
1 : 4
1 : 8
2 : 3
3 : 2
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
3
4.8 (24 rating)
LM
Lailatul Maghfiroh
Pembahasan lengkap banget
kt
kipli thembik
Mudah dimengerti
Y
Yamate
Bantu banget
SF
Syaira Fatiha Maula
Ini yang aku cari!
SM
Sasa Maulida
Makasih ❤️ Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia