Jadi, jawaban yang benar adalah C.
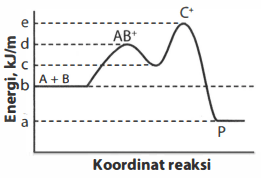
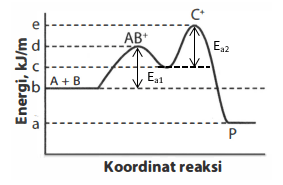
Pada soal, gambar profil energi membentuk dua puncak grafik yang mengindikasikan terdapat dua tahap reaksi. Reaksi pertama A+B→C dan reaksi kedua C→P. Dari grafik juga dapat diindikasikan nilai dari energi aktivasi (Ea). Energi aktivasi pada reaksi pertama (Ea1) memiliki nilai d-b, sedangkan energi aktivasi reaksi kedua (Ea2) memiliki nilai e-c. Nilai tetapan laju reaksi (k) berbanding terbalik dengan energi aktivasi, jika Ea↓ maka k↑ begitupula sebaliknya. Karena energi aktivasi yang besar menunjukkan kebutuhan energi yang lebih banyak atau dengan kata lain reaksi lebih sukar berjalan, sehingga nilai laju reaksi kecil. Besarnya Ea1 dan Ea2 hampir sama sehingga sulit ditentukan tahap penentu lajunya.
Peninjauan setiap pilihan jawaban:
Opsi A : Reaksi pembentukan P dari C merupakan tahap penentu laju reaksi.
Tahap penentu laju sebuah reaksi merupakan tahapan reaksi yang berjalan lebih lambat, yaitu reaksi yang memiliki nilai tetapan laju lebih kecil atau yang memiliki nilai energi aktivasi yang besar. Besarnya Ea1 dan Ea2 hampir sama sehingga sulit ditentukan tahap penentu lajunya tanpa mengetahui secara pasti nilai masing-masing energi aktivasi.
Opsi B : Pada temperatur yang sama, tetapan laju reaksi P dari C lebih besar dibanding tetapan laju reaksi pembentukan C dari A+B
Nilai tetapan laju reaksi (k) berbanding terbalik dengan energi aktivasi. Besarnya Ea1 dan Ea2 hampir sama sehingga sulit ditentukan tetapan laju reaksi yang lebih besar.
Opsi C : Senyawa antara C pasti akan dihasilkan jika sudah terbentuk senyawa teraktivasi AB+
Syarat terbentuknya suatu produk adalah dilewatinya energi aktivasi. Tanda suatu reaksi telah melampaui energi aktivasi adalah terbentuknya kompleks teraktivasi. Jika komplek teraktivasi AB+ telah terbentuk, maka produk antara C pasti akan terbentuk.
Opsi D : Produk P dapat dihasilkan dari reaksi antara A dan B dengan melewati satu senyawa teraktivasi
Pernyataan yang benar adalah produk P dapat dihasilkan dari reaksi antara A dan B dengan melewati DUA (bukan satu) senyawa teraktivasi yaitu AB+ dan C+.
Opsi E : A dan B dapat menghasilkan produk P tanpa pembentukan senyawa antara C.
Pernyataan yang benar adalah A dan B dapat menghasilkan produk P DENGAN (bukan tanpa) melalui pembentukan senyawa antara C.
Jadi, pernyataan yang benar adalah senyawa antara C pasti akan dihasilkan jika sudah terbentuk senyawa teraktivasi AB+.