Iklan
Pertanyaan
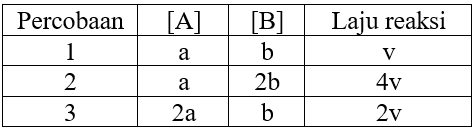
Perhatikan data percobaan penentuan laju reaksi dengan persamaan reaksi berikut. A + B → C Jika konsentrasi zat A tetap dan konsentrasi zat B dinaikkan dua kali dari semula, laju reaksi empat kali lebih cepat dari semula. Jika konsentrasi zat B tetap dan konsentrasi zat A dinaikkan dua kali dari semula, laju reaksi dua kali lebih cepat dari semula. Jika konsentrasi awal zat A = 2 mol/L dan konsentrasi zat B = 3 mol/L, besarnya laju reaksi adalah . . . .
Perhatikan data percobaan penentuan laju reaksi dengan persamaan reaksi berikut.
- Jika konsentrasi zat A tetap dan konsentrasi zat B dinaikkan dua kali dari semula, laju reaksi empat kali lebih cepat dari semula.
- Jika konsentrasi zat B tetap dan konsentrasi zat A dinaikkan dua kali dari semula, laju reaksi dua kali lebih cepat dari semula.
Jika konsentrasi awal zat A = 2 mol/L dan konsentrasi zat B = 3 mol/L, besarnya laju reaksi adalah . . . .
6
9
12
18
36
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
4
4.1 (12 rating)
yP
ydh Prt
Ini yang aku cari!
NA
Nazlia Andina
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia