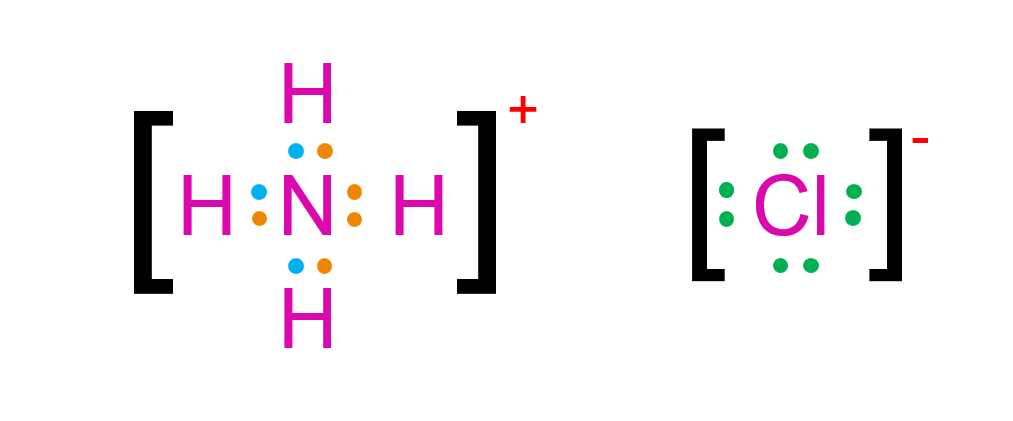Iklan
Pertanyaan
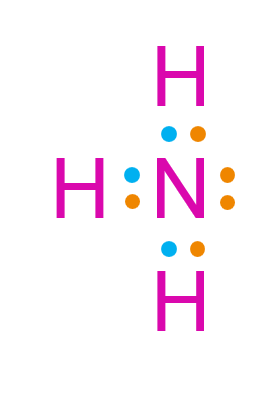
Pada senyawa NH 4 Cl terdapat ikatan...
Pada senyawa terdapat ikatan ...
kovalen dan ion
kovalen dan kovalen koordinasi
ion dan kovalen koordinasi
ion dan logam
kovalen, kovalen koordinasi, dan ion
Iklan
AA
A. Acfreelance
Master Teacher
Jawaban terverifikasi
1
4.9 (15 rating)
SN
Steven NNG
Makasih ❤️
Cu
Cahya ulandari
Pembahasan lengkap banget
N
Naana
Pembahasan lengkap banget Makasih ❤️
SZ
Syarifah Zahrah
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia