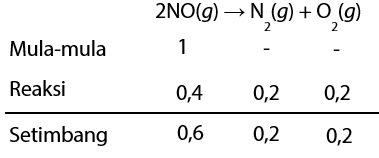Iklan
Pertanyaan
Pada ruang tertutup terdapat 1 mol gas NO yang terdisosiasi 40% menurut persamaan reaksi: 2 NO ( g ) → N 2 ( g ) + O 2 ( g ) Jika tekanan di dalam ruang tersebut 5 atm, maka nilai K p pada saat itu adalah ....
Pada ruang tertutup terdapat 1 mol gas yang terdisosiasi 40% menurut persamaan reaksi:
Jika tekanan di dalam ruang tersebut 5 atm, maka nilai pada saat itu adalah ....
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
2
4.0 (5 rating)
ar
aufa rafiqi
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia