Iklan
Pertanyaan
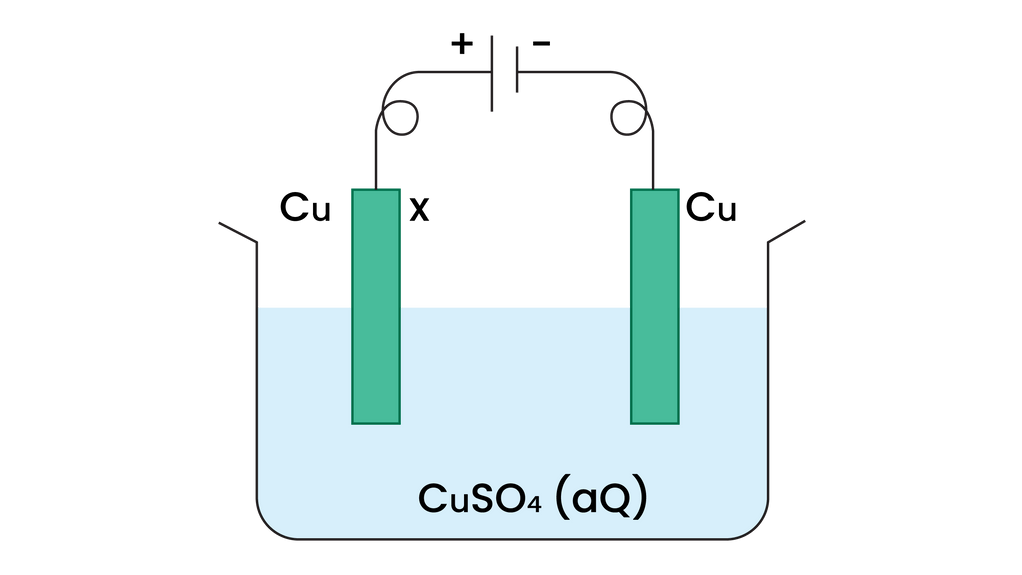
Pada elektrolisis seperti gambar di bawah ini, persamaan yang menunjukkan reaksi pada elektroda X adalah ...
Pada elektrolisis seperti gambar di bawah ini, persamaan yang menunjukkan reaksi pada elektroda X adalah ...
Iklan
AK
A. Kusbardini
Master Teacher
Mahasiswa/Alumni UIN Syarif Hidayatullah Jakarta
Jawaban terverifikasi
19
4.9 (21 rating)
TD
Triana Destiadi Supiyo
membantu dan jelas penjelasan nya
NH
Najwa Hawiya Humaira
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















