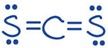Iklan
Pertanyaan
Nomor atom karbon dan belerang berturut-turut adalah 6 dan 16.Jika kedua atom tersebut membentuk senyawa, molekul senyawa tersebut ... Berbentuk linier Memiliki empat pasang elektron ikatan Mempunyai dua ikatan sigma dan dua ikatan pi Bersifat polar
Nomor atom karbon dan belerang berturut-turut adalah 6 dan 16. Jika kedua atom tersebut membentuk senyawa, molekul senyawa tersebut ...
- Berbentuk linier
- Memiliki empat pasang elektron ikatan
- Mempunyai dua ikatan sigma dan dua ikatan pi
- Bersifat polar
1, 2, dan 3 SAJA yang benar.
1 dan 3 SAJA yang benar.
2 dan 4 SAJA yang benar.
HANYA 4 yang benar.
SEMUA pilihan benar.
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia