Iklan
Pertanyaan
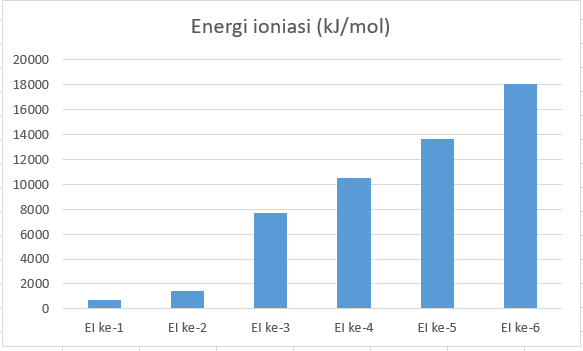
Nilai energi pengionan pertama sampai dengan keenam suatu unsur pada golongan utama berturut-turut adalah 738, 1.451, 7.733, 10.543, 13.630 dan 18.020 kJ/mol. Dari data tersebut dapat disimpulkan bahwa unsur tersebut cenderung membentuk ion bermuatan ....
Nilai energi pengionan pertama sampai dengan keenam suatu unsur pada golongan utama berturut-turut adalah 738, 1.451, 7.733, 10.543, 13.630 dan 18.020 kJ/mol. Dari data tersebut dapat disimpulkan bahwa unsur tersebut cenderung membentuk ion bermuatan ....
+1
+2
+3
+4
+5
Iklan
SL
S. Lubis
Master Teacher
Jawaban terverifikasi
2
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia