Iklan
Pertanyaan
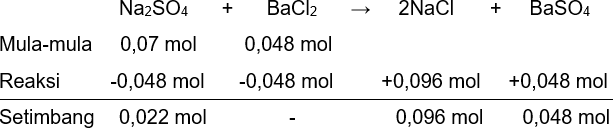
Larutan natrium sulfat dapat bereaksi dengan larutan barium klorida sesuai persamaan reaksi yang setara berikut: Na 2 SO 4 ( a q ) + BaCl 2 ( a q ) → 2 NaCl ( a q ) + BaSO 4 ( s ) Seorang siswa mencampurkan larutan yang mengandung 10,0 g Na 2 SO 4 dengan larutan yang mengandung 10,0 g BaCl 2 , dan diperoleh 12,0 g BaSO 4 . Persentase hasil (rendemen) dari reaksi ini adalah ...
Larutan natrium sulfat dapat bereaksi dengan larutan barium klorida sesuai persamaan reaksi yang setara berikut:
Seorang siswa mencampurkan larutan yang mengandung 10,0 g dengan larutan yang mengandung 10,0 g , dan diperoleh 12,0 g . Persentase hasil (rendemen) dari reaksi ini adalah ...
Iklan
AC
A. Chandra
Master Teacher
Mahasiswa/Alumni Universitas Negeri Jakarta
Jawaban terverifikasi
12
4.6 (18 rating)
CL
Cut Lis
Makasih ❤️
SR
Selvira Raisyfa
Makasih ❤️
SG
Septian Ghaza Maulana
Makasih ❤️
na
nur azizah
Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia