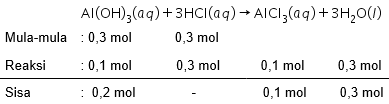Iklan
Pertanyaan
Larutan Al ( OH ) 3 2 M direaksikan dengan 150 mLlarutan HCl2 M menurut reaksi berikut. Al ( OH ) 3 ( a q ) + HCl ( a q ) → AICI 3 ( a q ) + H 2 O ( l ) ( belum setara ) Apabila volume larutan yang direaksikan sama dengan volume HCI, maka tentukan: a. zat yang berfungsi sebagai pereaksi pembatas; b. pereaksi yang berlebih.
Larutan 2 M direaksikan dengan 150 mL larutan HCl 2 M menurut reaksi berikut.
Apabila volume larutan yang direaksikan sama dengan volume HCI, maka tentukan:
a. zat yang berfungsi sebagai pereaksi pembatas;
b. pereaksi yang berlebih.
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
4
4.8 (5 rating)
Az
Alyya zhahira
Pembahasan lengkap banget
SZ
Salwa Zahratun Nisa
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Bantu banget Makasih ❤️
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia