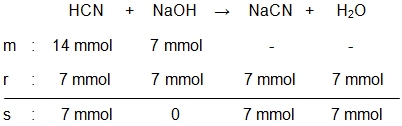Iklan
Iklan
Pertanyaan
Larutan 100 mL HCN 0,14 M dicampur dengan 70 mL NaOH 0,1 M, maka ... Reaksi yang terjadi: HCN + NaOH → NaCN + H 2 O Larutan NaOH merupakan reagen pembatas Larutan yang terjadi bersifat larutan penyangga pH larutan = 9 (UMPTN '01 Rayon B)
Larutan 100 mL HCN 0,14 M dicampur dengan 70 mL NaOH 0,1 M, maka ...
- Reaksi yang terjadi:
- Larutan NaOH merupakan reagen pembatas
- Larutan yang terjadi bersifat larutan penyangga
- pH larutan = 9
(UMPTN '01 Rayon B)
1, 2, dan 3 SAJA yang benar.
1 dan 3 SAJA yang benar.
2 dan 4 SAJA yang benar.
HANYA 4 yang benar.
SEMUA pilihan benar.
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
4
5.0 (1 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia