Iklan
Pertanyaan
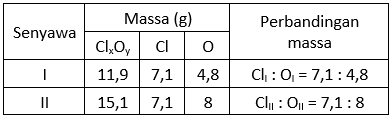
Klor bersenyawa dengan oksigen menghasilkan 2 macam senyawa. Pada senyawa I, jika klor 7,1 gram, maka massa senyawanya 11,9 gram. Pada senyawa II, jika klor = 7,1, massa senyawa = 15,1 gram. Buktikan hukum Dalton berlaku dan tulis rumus kimia senyawa yang terjadi!
Klor bersenyawa dengan oksigen menghasilkan 2 macam senyawa. Pada senyawa I, jika klor 7,1 gram, maka massa senyawanya 11,9 gram. Pada senyawa II, jika klor = 7,1, massa senyawa = 15,1 gram. Buktikan hukum Dalton berlaku dan tulis rumus kimia senyawa yang terjadi!
Iklan
Q'
Q. 'Ainillana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
2
2.0 (1 rating)
m
moonjuice
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia