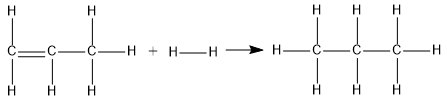Iklan
Pertanyaan
Jika diketahui ikatan energi rata-rata: H − H = 436 kj / mol C = C = 607 kj / mol C − H = 415 kj / mol C − C = 348 kj / mol Hitunglah △ H pada reaksi: C 3 H 6 ( g ) + H 2 ( g ) → C 3 H 8 ( g )
Jika diketahui ikatan energi rata-rata:
Hitunglah pada reaksi:
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
6
4.3 (20 rating)
MA
M. Ariq Azzaky Ankanka
Ini yang aku cari!
ER
Elvi Rahmi
Makasih ❤️
HA
Hikmah, A
Pembahasan lengkap banget Ini yang aku cari! Bantu banget Makasih ❤️ Mudah dimengerti
AA
Amanda Anindya
Bantu banget Makasih ❤️
k
kesya
Mudah dimengerti Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia