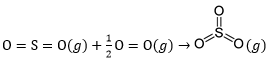Iklan
Pertanyaan
Jika diketahui energi ikatan S − O = 469 kJ mol − 1 , S = O = 323 kJ mol − 1 dan O = O = 495 kJ mol − 1 , hitunglah perubahan entalpi dari reaksi berikut: SO 2 ( g ) + 2 1 O 2 ( g ) → SO 3 ( g )
Jika diketahui energi ikatan , dan , hitunglah perubahan entalpi dari reaksi berikut:
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
18
4.6 (28 rating)
AI
Agung Indira
Ini yang aku cari!
W
Wahyuni
Makasih ❤️
KP
Kayla Putri Azzahra
Ini yang aku cari! Mudah dimengerti Makasih ❤️
AF
Alzena Faiq Nafiah
Mudah dimengerti Makasih ❤️ Bantu banget Ini yang aku cari! Pembahasan lengkap banget
NH
Nurul Hafifah Gea
Ini yang aku cari!
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia