Ikatan antar atom nonlogam yang terjadi melalui pemakaian pasangan elektron bersama disebut ikatan kovalen. Ikatan kovalen koordinasi adalah ikatan yang terbentuk dengan cara pemakaian bersama pasangan elektron yang berasal dari salah satu atom, ion atau molekul yang memiliki pasangan elektron bebas (PEB). Adapun atom, ion, molekul lain hanya menyediakan orbital kosong. Dengan kata lain, pada ikatan kovalen koordinasi ada satu atom yang berperan sebagai donor pasangan elektron dan satu atom sebagai akseptor pasangan elektron.
Pasangan elektron yang digunakan untuk ikatan kovalen koordinasi dapat digambarkan dengan anak panah (→) dengan arah dari donor menuju ke akseptor pasangan elektron. Ikatan kovalen koordinasi juga disebut ikatan semi polar atau ikatan dativ. Contoh senyawa dan ion yang mengandung ikatan kovalen koordinasi adalah ion NH4+ dan senyawa NH4Cl. Struktur Lewis dari ion NH4+ adalah sebagai berikut.
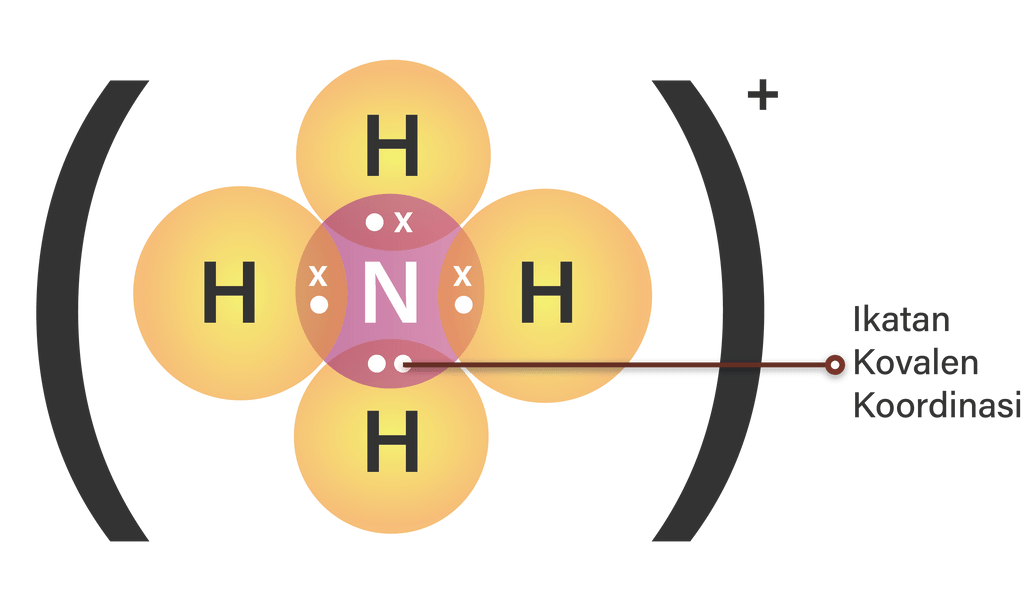
Senyawa amonia (NH3) memiliki sepasang elektron bebas (PEB), sedangkan pada ion H+, atom H telah kehilangan sebuah elektronnya. Oleh karena itu, sepasang elektron bebas dari senyawa NH3, selanjutnya digunakan bersama dengan ion H+ untuk membentuk ikatan kovalen koordinasi.
Dengan demikian, maka ikatan kovalen koordinasi dijumpai pada molekul ion NH4+.
Jadi, jawaban yang tepat adalah E.
















