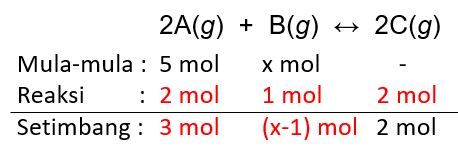Iklan
Pertanyaan
Harga Kc untuk reaksi: 2 A ( g ) + B ( g ) ⇌ 2 C ( g ) adalah 4 pada T ∘ C . Berapa mol B harus direaksikan dengan 5 mol A dalam suatu wadah 5 liter sehingga pada keadaan setimbang dapat membentuk 2 mol C?
Harga Kc untuk reaksi: adalah 4 pada . Berapa mol B harus direaksikan dengan 5 mol A dalam suatu wadah 5 liter sehingga pada keadaan setimbang dapat membentuk 2 mol C?
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
23
4.4 (5 rating)
V
Vincentlin
Ini yang aku cari!
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2025 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia