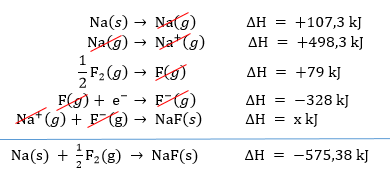Iklan
Pertanyaan
Gunakan bagan-bagan dari NaCl dan CaF 2 berikutuntuk menghitung soaldi bawah ini! Energi kisi adalah energi yang dilepas ion-ion dalam bentuk gas membentuk padatan kristalnya. Dimas ingin menghitung energi kisi NaF ( △ H f 0 NaF = − 575 , 38 kJ / mol ) tetapiDimas hanya memilikidata reaksi NaCl dan CaF 2 seperti gambar di atas. Kemungkinan usaha Dimas menghitung energi kisi NaF adalah ....
Gunakan bagan-bagan dari dan berikut untuk menghitung soal di bawah ini!

Energi kisi adalah energi yang dilepas ion-ion dalam bentuk gas membentuk padatan kristalnya. Dimas ingin menghitung energi kisi tetapi Dimas hanya memiliki data reaksi dan seperti gambar di atas. Kemungkinan usaha Dimas menghitung energi kisi adalah ....
bisa dilakukan,
bisa dilakukan,
tidak bisa dilakukan
bisa dilakukan,
bisa dilakukan,
Iklan
KK
K. Kak.Rachman
Master Teacher
Jawaban terverifikasi
5
5.0 (1 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia