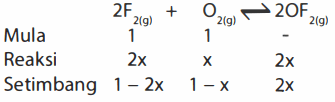Iklan
Pertanyaan
Gas oksigen difluorida ( OF 2 ) disintesis dari reaksi antara gas F 2 dengan gas O 2 menurut reaksi berikut: 2 F 2 ( g ) + O 2 ( g ) ⇌ 2 OF 2 ( g ) Dalam sebuah wadah dengan volume tertentu, tekanan awal gas F 2 dan gas O 2 diketahui masing-masing 1 atm. Jika pada kesetimbangan tekanan total gas adalah 1,75 atm maka nilai K p reaksi tersebut adalah ...
Gas oksigen difluorida () disintesis dari reaksi antara gas dengan gas menurut reaksi berikut:
Dalam sebuah wadah dengan volume tertentu, tekanan awal gas dan gas diketahui masing-masing 1 atm. Jika pada kesetimbangan tekanan total gas adalah 1,75 atm maka nilai reaksi tersebut adalah ...
0,133
0,278
0,555
0,755
1,333
Iklan
BR
B. Rohmawati
Master Teacher
Mahasiswa/Alumni Universitas Negeri Semarang
Jawaban terverifikasi
1
5.0 (5 rating)
RA
Reva Aurelia
Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia