Iklan
Pertanyaan
Gas Argon dianggap sebagai gas ideal. Gas itu mula-mula mempunyai energi dalam E i dan temperatur T i . Gas tersebut mengalami proses dengan melakukan usaha W . melepaskan energi senilai Q dan keadaan akhir energi dalam E f serta temperatur T f . Besarnya perubahan energi tersebut digambarkan seperti gambar berikut. Apa simpulan proses tersebut? (SBMPTN 2016)
Gas Argon dianggap sebagai gas ideal. Gas itu mula-mula mempunyai energi dalam Ei dan temperatur Ti. Gas tersebut mengalami proses dengan melakukan usaha W. melepaskan energi senilai Q dan keadaan akhir energi dalam Ef serta temperatur Tf. Besarnya perubahan energi tersebut digambarkan seperti gambar berikut.
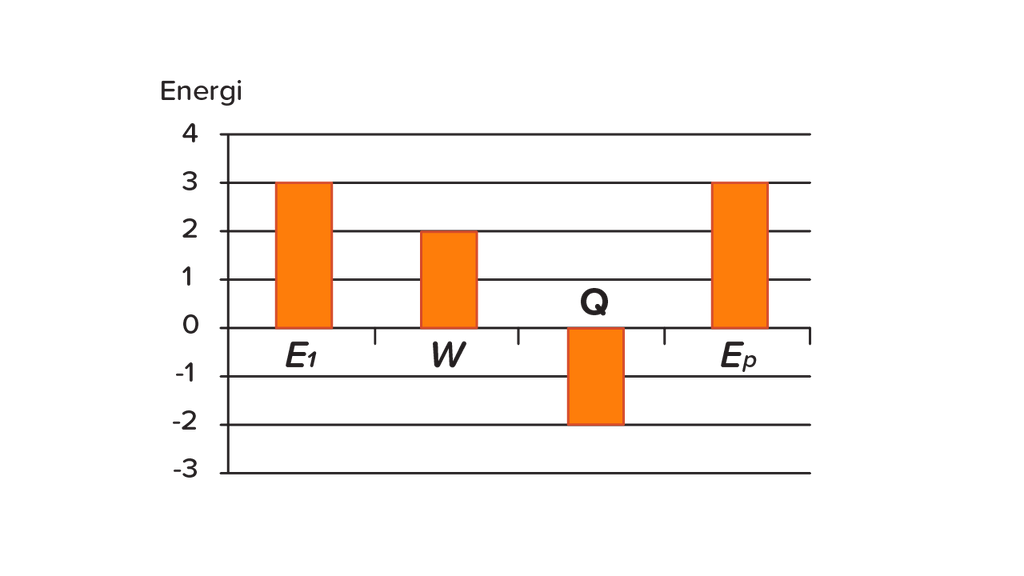
Apa simpulan proses tersebut?
(SBMPTN 2016)
Gas mengalami proses isobarik dan Tf < T1.
Gas mengalami proses adiabatik dan Tf < T1.
Gas mengalami proses isokhorik dan Tf < T1.
Gas mengalami proses isotermal dan Tf = T1.
Gas mengalami proses isokhorik dan Tf = T1.
Iklan
R. Maiza
Master Teacher
Mahasiswa/Alumni Institut Teknologi Bandung
1
5.0 (4 rating)
Lee Seung Gi
Keren
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia















