Menurut Teorema Ekipartisi Energi, Energi kinetik partikel gas dipengaruhi oleh temperatur gas dan derajat kebebasan partikel gas, yang dinyatakan ke dalam persamaan berikut ini:

f adalah drajat kebebasan partikel gas yang menyatakan banyaknya cara partikel gas bergerak. Sedangkan T adalah temperatur atau suhu gas. Persamaan itu menunjukkan bahwa suhu gas mempengaruhi energi kinetik partikel gas. Bentuk Energi kinetik yang dimiliki partikel gas ada beberapa macam, yaitu energi kinetik translasi, rotasi, dan vibrasi. Gas diatomik sendiri dapat bergerak secara translasi, rotasi, dan vibrasi seperti yang ditunjukkan pada gambar di bawah ini:
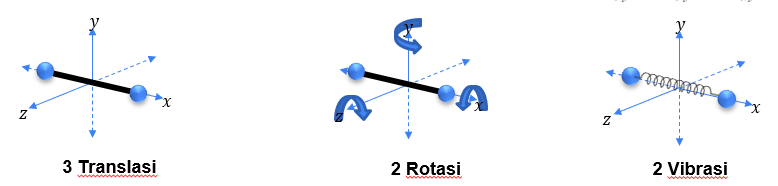
Sehingga, ketika gas diatomik tersebut mengalami kenaikan suhu, maka ketika bentuk energi kinetik tersebut akan mengalami peningkatan, yaitu peningkatan energi kinetik translasi, energi rotasi, dan energi vibrasi. sehingga pernyataan 2, 3, dan 4 benar.
Energi dalam pada gas ideal atau sering diberikan notasi U, merupakan jumlah energi kinetik total dari seluruh molekul gas dalam suatu ruangan, yang dirumuskan sbb:

Pada persaman itu terlihat bahwa Energi dalam gas sebanding dengan energi kinetik partikel gas. Sehingga, energi dalam gas diatomik tersebut juga akan meningkat karena energi kinetik partikel gas juga meningkat akibat kenaikan suhu gas. Sehingga, pernyataan 1 benar.
Jadi, pernyataan yang tepat adalah pernyataan nomor 1, 2, 3, dan 4.


















