Iklan
Pertanyaan
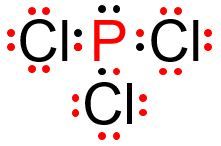
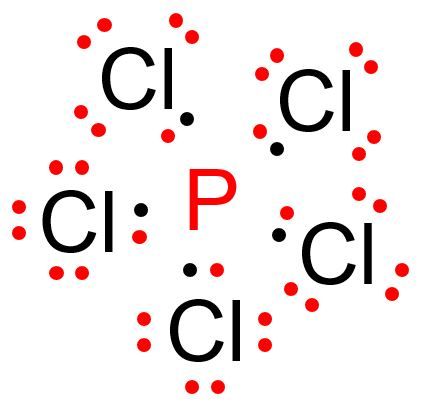
Diketahui nomor atom P = 15 dan nomor atom Cl = 17, bila kedua atom berikatan membentuk molekul PCI 3 dan PCI 5 . Buatlah langkah-langkah untuk menggambarkan bentuk molekul .
Diketahui nomor atom P = 15 dan nomor atom Cl = 17, bila kedua atom berikatan membentuk molekul . Buatlah langkah-langkah untuk menggambarkan bentuk molekul .
Iklan
ED
E. Dwihermiati
Master Teacher
Mahasiswa/Alumni Universitas Pendidikan Indonesia
Jawaban terverifikasi
5
4.8 (8 rating)
al
ayunia laloan
Pembahasan lengkap banget Ini yang aku cari!
SR
Sinta Rahayuu
Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia