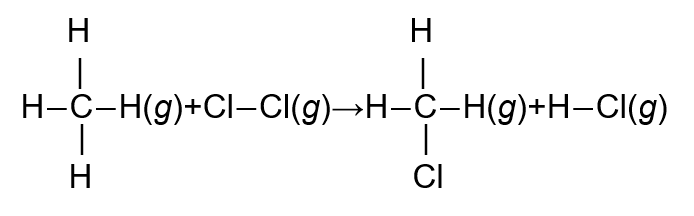Iklan
Pertanyaan
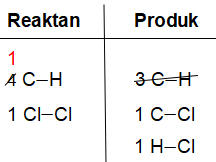
Diketahui energi ikatan rata-rata sebagai berikut. C − H Cl − Cl C − Cl H − Cl H − H = = = = = 414 kJ / mol 244 kJ / mol 326 kJ / mol 431 kJ / mol 436 kJ / mol Nilai perubahan entalpi untuk reaksi pembentukan 0,1 mol gas metil klorida ( CH 3 Cl )dari gas metana dan gas klorin menghasilkan produk samping gas asam klorida adalah …
Diketahui energi ikatan rata-rata sebagai berikut.
Nilai perubahan entalpi untuk reaksi pembentukan 0,1 mol gas metil klorida () dari gas metana dan gas klorin menghasilkan produk samping gas asam klorida adalah …
99 kJ
99 kJ
9,9 kJ
14,5 kJ
145 kJ
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
3
5.0 (2 rating)
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia