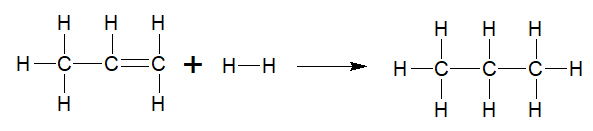Iklan
Pertanyaan
Diketahui energi ikatan rata-rata: C = C = 839 kJ / mol C − C = 343 kJ / mol H − H = 436 kJ / mol C − H = 410 kJ / mol Perubahan entalpi yang terjadi pada reaksi: CH 3 − CH = CH 2 + H 2 → CH 3 − CH 2 − CH 3 sebesar ....
Diketahui energi ikatan rata-rata:
Perubahan entalpi yang terjadi pada reaksi:
sebesar ....
+548 kJ/mol
+271 kJ/mol
+112 kJ/mol
-112 kJ/mol
-548 kJ/mol
Iklan
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
20
4.4 (19 rating)
YA
Yuprizal Apryandi
Ini yang aku cari!
BM
Brema Mamana
Ini yang aku cari!
KS
Komang Saraswati
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia