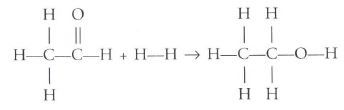Iklan
Pertanyaan
Diketahui energi ikatan rata-rata: C − H = 414 kJ / mol C − C = 346 kJ / mol C = O = 740 kJ / mol C − O = 357 kJ / mol H − H = 436 kJ / mol O − H = 464 kJ / mol Perubahan entalpi reaksi: adalah ....
Diketahui energi ikatan rata-rata:
Perubahan entalpi reaksi:
adalah ....
-2.410 kJ/mol
-241 kJ/mol
-59 kJ/mol
+59 kJ/mol
+2.410 kJ/mol
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
12
4.6 (26 rating)
CA
Clarissa Aulia Nugraha
Makasih ❤️ Bantu banget
MI
Muamar Idham Kholid
Pembahasan lengkap banget
AS
Andi Siti Batara Shinta
Makasih ❤️
KP
Kayla Putri Azzahra
Pembahasan lengkap banget
RK
Rayya Khairunnisa Ghassani
Pembahasan lengkap banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia