Iklan
Pertanyaan
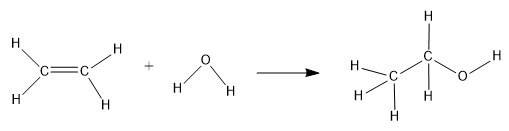
Diketahui energi ikatan rata-rata dalam kJ/mol dari: C=C : 607 C-C : 343 C-H : 410 O-H : 460 C-O : 351 Perubahan entalpi dari reaksi: CH 2 = CH 2 + H 2 O → CH 3 − CH 2 − OH adalah ....
Diketahui energi ikatan rata-rata dalam kJ/mol dari:
C=C : 607
C-C : 343
C-H : 410
O-H : 460
C-O : 351
Perubahan entalpi dari reaksi:
adalah ....
-111 kJ/mol
+111 kJ/mol
-37 kJ/mol
+37 kJ/mol
-74 kJ/mol
Iklan
NP
N. Puspita
Master Teacher
Jawaban terverifikasi
2
4.5 (19 rating)
AD
Audina Dewi Ramadhani
Makasih ❤️
SS
Siliman Samaros Adadikam
Makasih ❤️
F
Fian
Makasih ❤️
JD
Jesika Dumatubun
Pembahasan tidak menjawab soal
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia