Iklan
Pertanyaan
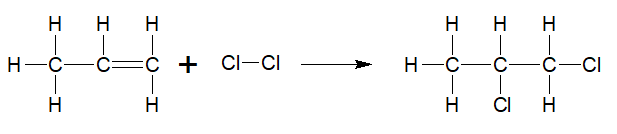
Dengan menggunakan data energi ikatan berikut. C=C = 612 kJ/mol Cl-Cl = 243 kJ/mol C-C = 347 kJ/mol C-Cl = 346 kJ/mol Tentukan △ H reaksi: C 3 H 6 + Cl 2 → C 3 H 6 Cl 2
Dengan menggunakan data energi ikatan berikut.
C=C = 612 kJ/mol
Cl-Cl = 243 kJ/mol
C-C = 347 kJ/mol
C-Cl = 346 kJ/mol
Tentukan reaksi:
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
5
4.6 (9 rating)
el
emiriliana lolyta
Pembahasan tidak lengkap Pembahasan terpotong Ini yang aku cari!
R
RachelSiallgn
Jawaban tidak sesuai
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia