Iklan
Iklan
Pertanyaan
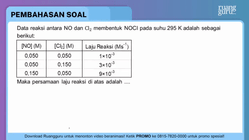
Data reaksi antara NO dan Cl 2 membentuk NOCI pada suhu 295 K adalah sebagai berikut: Maka persamaan laju reaksi di atas adalah ....
Data reaksi antara NO dan membentuk NOCI pada suhu 295 K adalah sebagai berikut:
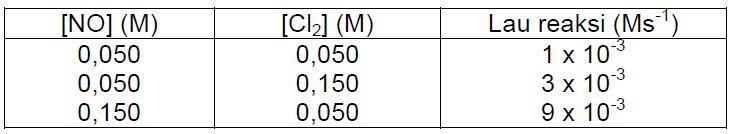
Maka persamaan laju reaksi di atas adalah ....
Iklan
AA
A. Acfreelance
Master Teacher
Jawaban terverifikasi
3
0.0 (0 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia