Iklan
Pertanyaan
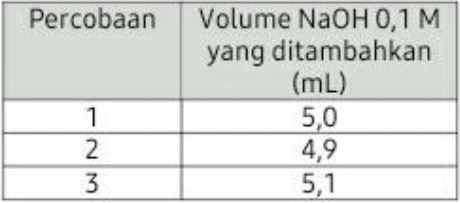
Data hasil titrasi 10 mL H 2 SO 4 dengan NaOH 0,1 M sebagai berikut. Besarnya konsentrasi yang bereaksi adalah ....
Data hasil titrasi 10 mL dengan NaOH 0,1 M sebagai berikut.
Besarnya konsentrasi yang bereaksi adalah ....
0,025 M
0,05 M
0,005 M
0,25 M
2,5 M
Iklan
FH
F. Handiani
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
19
4.8 (20 rating)
C
Cika
Pembahasan lengkap banget
FB
Faizah Balita Masruri
Makasih ❤️ Ini yang aku cari! Bantu banget
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia